Каталог товаров
Каталог товаров
Бактробан (Мупироцин), мазь назал. 20мг/г
- Код товара:
- 68388
- Производитель:
- Смит Кляйн Бичем (Испания)
- Наличие:
- На складе
- Цена со скидкой:
- 180,00 грн
Альфарекин (alpharekin), лиофил. пор. д/ин. 1 млн МЕ, №10
- Код товара:
- 68836
- Производитель:
- Интерфармбиотек (Украина)
- Годен до:
- 01.05.2027
- Наличие:
- Есть в наличии
- Цена:
- 1 650,00 грн
Альфарекин (alpharekin), лиофил. пор. д/ин. 1 млн МЕ, №10
- Код товара:
- 2011095
- Производитель:
- Интерфармбиотек (Украина)
- Годен до:
- 01.05.2027
- Наличие:
- Есть в наличии
- Цена:
- 1 650,00 грн
Визан (Vizan), табл. 2 мг, №28
- Код товара:
- 1011981
- Производитель:
- Schering GmbH & Co. Productions (Германия)
- Годен до:
- 01.11.2029
- Наличие:
- Есть в наличии
- Цена:
- 1 064,00 грн
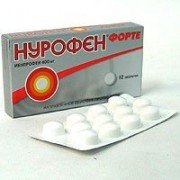
Нурофен форте, табл. по 400 мг, №12
- Код товара:
- 22772
- Производитель:
- Reckitt Benckiser Healthcare International (Великобритания)
- Годен до:
- 01.12.2027
- Наличие:
- Есть в наличии
- Цена:
- 168,00 грн
Ортофен, табл. по 25 мг, №30
- Код товара:
- 29609
- Производитель:
- Здоровье (Украина)
- Наличие:
- Есть в наличии
- Цена:
- 25,00 грн
Оспамокс, табл. по 500 мг, №12
- Код товара:
- 29781
- Производитель:
- Sandoz (Австрия)
- Годен до:
- 01.11.2028
- Наличие:
- Есть в наличии
- Цена:
- 212,00 грн
Оспамокс, табл. по 500 мг, №12
- Код товара:
- 1004047
- Производитель:
- Sandoz (Австрия)
- Годен до:
- 01.11.2028
- Наличие:
- Есть в наличии
- Цена:
- 212,00 грн
Реополиглюкин, р-р инф. бут. 200 мл
- Код товара:
- 68019
- Производитель:
- Юрия-Фарм (Украина)
- Годен до:
- 01.03.2027
- Наличие:
- Есть в наличии
- Цена:
- 224,00 грн
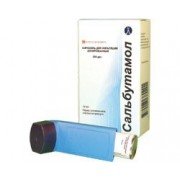
Сальбутамол, аэр. 100 мкг/доза 200 доз, №1
- Код товара:
- 34624
- Производитель:
- GlaxoSmithKline Pharmaceuticals (Польша)
- Наличие:
- Есть в наличии
- Цена:
- 107,00 грн
Есть в наличии - есть в аптеке или может быть доставлен в аптеку в течение суток от поставщиков или с других аптек сети
На складе - доставка товара осуществляется курьерскими службами со склада